关键词:CD34+ 造血干细胞 ;CD34+ 祖细胞;CD34+造血干细胞/祖细胞;骨髓CD34+造血干细胞/祖细胞;脐带血CD34+造血干细胞/祖细胞;动员外周血造血干细胞/祖细胞;外周血CD34+造血干细胞/祖细胞;造血微环境;造血重建;骨髓移植;基因编辑;靶向递送;造血分化;免疫重建;CD34+ Hematopoietic Stem and Progenitor Cells, CD34+ HSPCs;Bone Marrow CD34+ Hematopoietic Stem and Progenitor Cells,BM CD34+ HSPCs;Umbilical Cord Blood CD34+ Hematopoietic Stem and Progenitor Cells,UCB CD34+ HSPCs;Mobilized Peripheral Blood Hematopoietic Stem and Progenitor Cells ,mPB HSPCs;Peripheral Blood CD34+ Hematopoietic Stem/Progenitor Cells ,PB CD34+ HSPCs;Hematopoietic Niche;
CD34+ 造血干细胞/祖细胞(CD34+ Hematopoietic Stem and Progenitor Cells, CD34+ HSPCs)是造血系统中具有自我更新与多向分化潜能的核心种子细胞,主要定位于骨髓造血微环境(Hematopoietic Niche),同时少量存在于外周血及脐带血中,承担着维持机体造血稳态、修复造血损伤及重建免疫功能的关键使命。随着单细胞测序、基因编辑、细胞工程等技术的飞速发展,CD34+ HSPCs的研究已从基础生物学特性解析,逐步延伸至造血调控机制、疾病发病机制及临床转化应用等多个前沿领域,成为血液系统疾病、遗传性疾病治疗及再生医学发展的核心突破口。因此,合格的CD34+造血干细胞/祖细胞(CD34+ Hematopoietic Stem and Progenitor Cells, CD34+ HSPCs)尤为重要。IPHASE作为体外研究生物试剂领域的领-军企业,具备合规且优质的人动员外周血CD34+造血干细胞/祖细胞(Mobilized Peripheral Blood Hematopoietic Stem and Progenitor Cells, mPB HSPCs)、人外周血CD34+造血干细胞/祖细胞(Peripheral Blood CD34+ Hematopoietic Stem/Progenitor Cells ,PB CD34+ HSPCs)及人脐带血CD34+造血干细胞/祖细胞(Umbilical Cord Blood CD34+ Hematopoietic Stem and Progenitor Cells, UCB CD34+ HSPCs)资源,为相关领域的后续研究与临床应用提供了卓-越的基础材料支持。
01 CD34+造血干细胞 / 祖细胞的生物学特性
CD34+ HSPCs 是一类表达 CD34 表面抗原、具有自我更新与多向分化潜能的成体干细胞群体,主要定位于骨髓造血微环境(Hematopoietic Niche)中,同时少量存在于外周血和脐带血中。其核心功能贯穿造血稳态维持、造血损伤修复及免疫重建三大维度,其生物学行为受到精密的分子调控网络与微环境信号的协同调控。
(一)核心生物学功能
自我更新能力:CD34+ HSPCs 能够通过不对称分裂或对称分裂,在维持自身干细胞特性与数量稳定的同时,持续产生子代细胞,为长期造血提供源源不断的 “细胞储备",这是其区别于成熟造血细胞的关键特征。
多向分化潜能:在特定细胞因子、转录因子及微环境信号的调控下,CD34+ HSPCs 可定向分化为髓系(粒细胞、单核细胞、红细胞、血小板)和淋系(T 淋巴细胞、B 淋巴细胞、自然杀伤细胞)两大谱系的各类成熟血细胞,完成造血谱系的全面重建。
造血重建功能:当机体遭遇化疗、放疗、造血功能衰竭等损伤时,CD34+ HSPCs 可被激活并迁移至损伤部位,增殖分化为各类成熟血细胞,快速恢复机体造血功能与免疫防御能力,这是其临床应用的核心基础。
(二)组织分布与亚群特性
CD34+ HSPCs 在不同组织中的分布具有显著差异,其生物学特性也存在一定的 “来源特异性",直接影响其临床应用效果。
【细胞来源】解剖位置
【骨髓CD34+ HSPCs】骨髓造血微环境内
【脐带血CD34+ HSPCs】新生儿脐带血中
【动员外周血CD34+ HSPCs】经动员的外周血液循环中
【细胞来源】细胞特性
【骨髓CD34+ HSPCs】自我更新能力强,增殖分化潜能稳定,长期造血重建能力突出,细胞活性高
【脐带血CD34+ HSPCs】免疫原性低,增殖活性高,对供受者配型要求宽松,获取便捷且无-创伤
【动员外周血CD34+ HSPCs】获取便捷,创伤小,细胞纯度较高,短期造血重建能力强
【细胞来源】分化倾向
【骨髓CD34+ HSPCs】髓系与淋系分化平衡,免疫重建效果稳定
【脐带血CD34+ HSPCs】更倾向于髓系分化,造血恢复速度稍慢于外周血来源
【动员外周血CD34+ HSPCs】髓系分化优势明显,造血恢复速度快,长期造血重建能力略弱于骨髓来源
【细胞来源】临床意义
【骨髓CD34+ HSPCs】造血干细胞移植的“金标准"来源,适用于各类血液系统疾病、免疫缺陷病的异基因或自体移植
【脐带血CD34+ HSPCs】适合儿童及低体重患者移植,可作为骨髓移植的替代选择,也可用于多份脐带血联合移植治疗成人患者
【动员外周血CD34+ HSPCs】常用于自体造血干细胞移植(如肿瘤患者放化疗后),也可用于异基因移植的辅助治疗,降低移植相关并发症
此外,CD34+ HSPCs群体存在显著的异质性,可根据表面标志物的表达差异(如CD38、CD90、CD45RA等)分为不同亚群,其中“CD34+ CD38- CD90+"亚群的自我更新能力与造血重建潜能最-强,被认为是最-接近原始造血干细胞的群体,也是目前基础研究与临床应用的核心靶标亚群。
02 CD34+造血干细胞 / 祖细胞的研究与应用
CD34+ HSPCs 的研究已从最初的细胞生物学特性解析,逐步扩展至造血调控机制、疾病模型构建、细胞治疗、基因治疗等多个前沿领域,其临床应用也从传统的骨髓移植逐步向精准治疗、再生医学等方向拓展,推动着临床医学的范式革新。
(一)基础研究领域
造血调控机制解析:当前研究聚焦于 CD34+ HSPCs 自我更新与分化平衡的分子调控网络,包括表观遗传修饰(DNA 甲基化、组蛋白修饰)、非编码 RNA 调控、细胞外基质与造血微环境的相互作用等。通过单细胞转录组学、空间转录组学等技术,深入挖掘调控 CD34+ HSPCs 命运决定的关键分子靶点,为疾病治疗提供理论基础。
疾病发病机制研究:CD34+ HSPCs 功能异常与多种血液系统疾病密切相关。例如,白血病干细胞本质上是发生基因突变的异常 CD34+ HSPCs,其自我更新能力异常增强、分化受阻,导致恶性增殖;再生障碍性贫血、骨髓增生异常综合征等疾病中,CD34+ HSPCs 的增殖分化能力下降,引发造血功能衰竭。通过解析这些疾病中 CD34+ HSPCs 的分子异常,可为疾病诊断与治疗提供新的思路。
造血微环境互作研究:造血微环境(Hematopoietic Niche)(又称 “造血龛")是维持 CD34+ HSPCs 功能稳定的关键环境,包括成骨细胞、内皮细胞、间充质干细胞等细胞成分及细胞因子、细胞外基质等非细胞成分。研究 CD34+ HSPCs 与造血微环境的相互作用机制,对于理解造血稳态维持、造血损伤修复及疾病发生发展具有重要意义。
(二)临床应用领域
造血干细胞移植:这是 CD34+ HSPCs 最-成熟的临床应用,已成为治疗白血病、淋巴瘤、多发性骨髓瘤、再生障碍性贫血等血液系统疾病的核心手段。通过移植健康的 CD34+ HSPCs,替代患者受损或异常的造血系统,实现造血功能与免疫功能的重建。根据供体来源,可分为自体移植、异基因移植(骨髓移植、脐带血移植、外周血造血干细胞移植),适用于不同类型的患者。
基因治疗载体:CD34+ HSPCs 具有长期自我更新与多向分化潜能,是基因治疗的理想载体。对于镰状细胞贫血、β- 地中海贫血、严重联合免疫缺陷病等遗传性疾病,可通过慢病毒载体、逆转录病毒载体等将正常基因导入 CD34+ HSPCs 中,再将修饰后的细胞回输患者体内,使其持续产生正常的血细胞,达到根-治疾病的目的。近年来,基因编辑技术(如 CRISPR-Cas9)的应用进一步提升了 CD34+ HSPCs 基因治疗的精准性与安全性,为遗传性疾病治疗带来了新的突破。
免疫重建与再生医学:在接受放化疗的肿瘤患者中,CD34+ HSPCs 移植可快速恢复其造血功能与免疫功能,降低感染、出血等并发症的风险;在免疫缺陷病患者中,CD34+ HSPCs 可分化为各类免疫细胞,重建机体免疫防御体系。此外,CD34+ HSPCs 还可用于造血损伤修复(如放射损伤、化学毒物损伤)、组织再生(如血管再生)等领域,展现出广阔的再生医学应用前景。
靶向药物递送平台:CD34+ HSPCs 具有向造血组织定向归巢的特性,可作为靶向药物递送的 “载体细胞"。通过将药物、纳米颗粒或免疫调节剂负载于CD34+ HSPCs 中,利用其归巢能力将治疗剂精准递送至骨髓等造血部位,提高药物在靶组织的浓度,降低全身毒性。这一策略在白血病、骨髓转移癌等疾病的治疗中具有潜在应用价值,是当前靶向治疗研究的热点方向之一。
03 IPHASE相关产品
依托CD34+ HSPCs在基础研究、临床诊疗领域的核心价值,以及行业对标准化、高质量相关产品的迫切需求,IPHASE作为体外研究生物试剂引-领者,紧跟时局,成功研发、生产出合规且优质的人动员外周血CD34+造血干细胞/祖细胞(Mobilized Peripheral Blood Hematopoietic Stem and Progenitor Cells, mPB HSPCs)、人外周血CD34+造血干细胞/祖细胞(Peripheral Blood CD34+ Hematopoietic Stem/Progenitor Cells ,PB CD34+ HSPCs)及人脐带血CD34+造血干细胞/祖细胞(Umbilical Cord Blood CD34+ Hematopoietic Stem and Progenitor Cells, UCB CD34+ HSPCs),并对其进行了纯度质控,实现了该核心细胞群体从科研到应用的产品化落地。
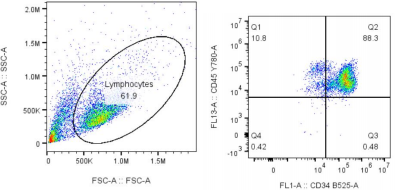
图片 IPHASE 人脐带血CD34+造血干细胞
电话
微信扫一扫
